éter
(< lat aether < gr α)
-
s
m
Espacio celeste.
-
s
m
[FÍS]
Substancia fluída, invisible, elástica, de existencia hipotética, que se supoñía en repouso absoluto, que penetraba toda a materia existente e todo o espacio, e á que se lle outorgaban propiedades contraditorias, como por exemplo a sutilidade, imponderabilidade ou elasticidade. Nela propagábanse as ondas electromagnéticas, desenvolvíanse os fenómenos ópticos ou transmitíase a calor e outras formas de enerxía. A teoría do éter, vixente no s XIX, era coherente coa física ondulatoria e mecánica daqueles tempos. A crenza nun espazo e nun tempo absolutos comportaba a existencia dun sistema de referencia privilexiado, asociado ao éter, e en repouso absoluto, respecto ao que eran válidas as ecuacións de Maxwell e en que se propagaban as ondas electromagnéticas. A teoría da relatividade puxo fin á idea do éter e demostrou que as ecuacións de Maxwell eran válidas en calquera sistema de referencia inercial.
-
[QUÍM]
-
s
m
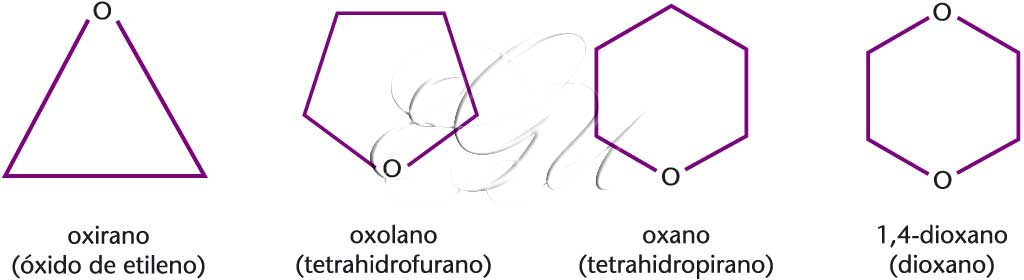
Nome xenérico das substancias orgánicas que se caracterizan pola presenza do grupo funcional -O-, onde un átomo de osíxeno está unido a dous radicais hidrocarbonados (aromáticos ou non). Nos éteres cíclicos, o átomo de osíxeno está unido a dous átomos de carbono que forman parte dunha cadea alifática pechada. Os éteres (R-O-R’) resultan da substitución de dous hidróxenos de auga por dous grupos alquilo, e son xeometricamente semellantes á auga e aos alcois. Segundo as normas da IUPAC, os éteres alifáticos desígnanse por medio do grupo RO- (alcoxi), que se considera como un substituínte da cadea máis longa, como o metoxietano. Tamén se poden designar por medio dos nomes dos radicais que van unidos ao átomo de osíxeno; en primeiro lugar o de menor número de átomos de carbono, seguidos da palabra éter, como por exemplo metil etil éter. Son bos disolventes para a maioría das substancias orgánicas, pero disolven moi pouco os compostos inorgánicos; por esta razón, os éteres son uns excelentes disolventes de uso comercial e de laboratorio, en especial para os procesos de extracción. Os éteres son inertes en presenza de bases, pero reaccionan en presenza de ácidos. A reacción máis importante que experimentan é a ruptura do enlace C-O. Esta reacción de ruptura é catalizada por ácidos, normalmente HI e, en menor medida, HBr ou HCl, pero neste caso son necesarias concentracións e temperaturas máis elevadas. Obtéñense xeralmente por reacción dun alcol con haloxenuros de alquilo, que se coñece como síntese de Williamson. Tamén se poden formar por un desprazamento S<J>N</J>2 de alcoholatos ou de fenóxidos sobre os haloxenuros de alquilo: RO - Na + +R’X→R-O-R’+NaX, onde R pode ser un grupo alquilo o un grupo fenilo, R’ é un alquilo primario ou secundario e X é I, Br ou Cl. Os alcois primarios e secundarios pódense metilar con diazometano, empregando como catalizador un ácido de Lewis, como o BF 3 , que ten por misión incrementar a acidez do alcol. Os fenois, que son máis ácidos, pódense metilar con diazometano sen necesidade de catalizador. Os éteres simétricos obtéñense a partir de alcois primarios por deshidratación con ácido sulfúrico concentrado. Os diois, ao deshidratarse, dan éteres cíclicos.
-
éter coroa
Éter cíclico que contén múltiples funcións éter e que presenta unha gran capacidade para captar ións metálicos e facelos solubles en disolventes orgánicos. Os éteres coroa noméanse a forma x-coroa-y, onde x representa o número total de átomos do anel e y é o número de osíxenos. Teñen importancia como catalizadores. Denomínanse así porque adoptan -en estado cristalino e, posiblemente, en solución- unha configuración semellante á dunha coroa.
-
éter de petróleo
Mestura de hidrocarburos saturados, principalmente pentanos e hexanos, que proceden das fraccións volátiles da destilación de petróleo. Acostúmase indicar o intervalo do punto de ebulición da mestura en cuestión; así, por exemplo, éter de petróleo 40-60°C. Os éteres de petróleo empréganse moito como disolventes apolares. Malia o seu nome, non teñen a función éter.
-
éter dimetílico [metoximetano: CH 3 OCH 3 ]
Gas inflamable, incoloro, soluble en auga e solventes orgánicos. Emprégase, entre outras cousas, como refrixerante, disolvente, axente de extracción, propelente para polvorizadores, medio de reacción ou gas de soldadura.
-
éter etílico/dietílico/sulfúrico [etoxietano: C 2 H 5 OC 2 H 5 ]
Líquido incoloro, moi volátil e inflamable, pouco soluble en auga, que constitúe o éter máis importante. Exposto ao aire, ao igual ca os outros éteres, forma peróxidos non volátiles que permanecen como residuos explosivos ao evaporarse o éter; para evitalo, os éteres comerciais levan un pouco de alcohol etílico e pequenas cantidades de auga. Industrialmente prepárase por acción do ácido sulfúrico concentrado sobre o etanol a 140°C, ou tamén sobre o etileno. É un dos disolventes de substancias orgánicas que máis se empregan na industria e nos laboratorios; especialmente, neste último caso, nos procesos de extracción de hormonas e de principios activos de plantas e tecidos. Administrado por inhalación, foi un dos anestésicos que máis se utilizou para operacións cirúrxicas longas, pero substituíuse por outros compostos debido aos seus efectos secundarios, como irritación do sistema respiratorio e náuseas.
-
s
m