átomo
(< lat atŏmu < gr
-
[FÍS]
-
s
m
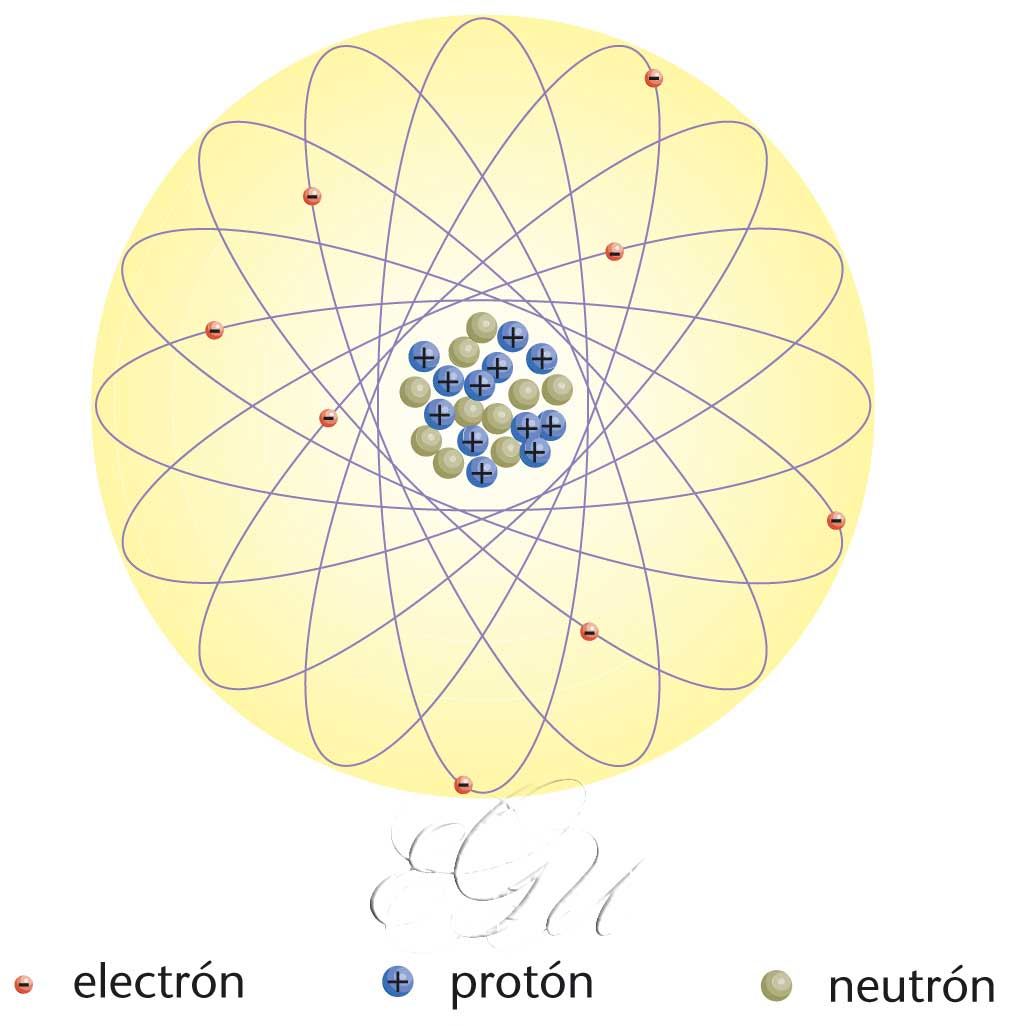
s m Sistema formado por un determinado número de partículas elementais (esencialmente protóns, neutróns e electróns) que, sendo electricamente neutros, posúe intrinsecamente as características dun elemento químico e non é a cantidade máis pequena que pode intervir nunha combinación química. Basicamente un átomo consta de dúas partes. Dunha banda o núcleo, formado por protóns e neutróns, que contén case toda a masa do átomo (99,9%), pero que só ocupa unha parte ínfima. Os electróns, doutra banda, envolven o núcleo formando capas a diferentes niveis e, a consecuencia da súa carga eléctrica negativa, neutralizan a carga positiva do núcleo. Os átomos dun mesmo elemento teñen o mesmo número de protóns e electróns (número atómico, Z), feito que determina as propiedades químicas do elemento. Non obstante , poden ter diferente número de neutróns (número neutrónico, N) no núcleo. Son os isótopos do elemento, que teñen propiedades físicas diferentes. Para distinguilos, cabe especificar o número de masa, (A=Z+N), que dá o número total de nucleóns (protóns e neutróns) do núcleo e que, multiplicado pola masa dun protón dá, aproximadamente, o peso do átomo (expresado en unidades de masa atómica) ou peso atómico (tamén denominada masa atómica). A clasificación dos elementos de acordo co número atómico (táboa periódica) evidencia unha periodicidade de propiedades. Os átomos raramente se atopan libres, independentes, senón que tenden a agruparse formando moléculas, das cales está formada toda a materia.
Evolución do concepto de átomo
Segundo a concepción atómica formulada na India no s VII a C, os átomos elementais eran cinco: o vital e os catro átomos fomadores (terra, aire, lume e auga) que combinados constitúen todas as cousas. En Grecia, cara ao ano 450 a C, Leucipo de Mileto estableceu a teoría de que a materia estaba constituída por pequenas unidades materiais, os átomos. Esta concepción foi retomada por Demócrito de Abdera e Epicuro. En Roma, Lucrecio (94-54 a C) continuou a tradición atomística grega na súa obra De Rerum Natura. Na Idade Media produciuse un retroceso do atomismo, ao imporse a alquimia, que intuíu a transmutación da materia e investigou a conversión dos metais en ouro coa axuda da pedra filosofal. Gassend aceptou a existencia do baleiro e Boyle chegou á conclusión de que os gases deben de ser constituídos por corpúsculos que se despracen. En 1774 Lavoisier enunciou a Lei da conservación da masa nas reaccións químicas. En 1799, J. L. Proust estableceu a Lei das proporcións definidas, que foi corroborada máis tarde por Berzelius. En 1804, J. Dalton enunciou a Lei das proporcións múltiples e introduciu os fundamentos da teoría atómica moderna. Desde 1805 ata 1809, J. L. Gay-Lussac enunciou a Lei dos volumes de combinación. En 1811 A. Avogadro enunciou a súa lei e W. Prout propuxo en 1815 que os átomos eran aglomerados de átomos de hidróxeno, hipótese despois rexeitada. Experimentando coa electrólise, Faraday deduciu en 1834 que cada átomo debía de posuír unha mesma cantidade de electricidade. En 1874, Stoney supuxo que na electrólise cada átomo transportaba a mesma carga eléctrica. En 1858 J. Plücker descubriu os raios catódicos, que J. Jittorf estudiou detidamente. En 1876, E. Goldstein mostrou que estes raios eran desviados por campos magnéticos e J. P. Perrin descubriu en 1895 que tranportaban carga eléctrica negativa e determinou a relación carga-masa destas hipotéticas partículas. J. J. Thomson (1897) apuntou a existencia dunha partícula elemental de carga eléctrica negativa, que foi denominada electrón. As observacións que desde 1886 fixo Goldstein sobre os raios canais e as experiencias cos campos magnéticos que fixo W. Wien en 1898, indicaron a existencia dunha carga elemental positiva, con carga igual á do electrón pero con signo oposto: o protón.
O modelo atómico de Bohr-Rutherford
Perrin propuxo en 1901 que o átomo era como un pequeno sistema solar, os electróns orbitan sobre unha partícula central positiva, idea que tamén seguiu H. Nagaoka. J. J. Thomson (1903) describiu o átomo como unha esfera cargada positivamente sobre a que se agrupaban os electróns, oscilando no contorno do centro e neutralizando a carga. Aproveitando o descubrimento da radioactividade por Becquerel (1896), entre 1908 e 1909, H. Geiger, E. Marsden e E. Rutherford fixeron experiencias de bombardeos dunha película de ouro con partículasα, a partir das que Rutherford concluíu en 1911 que o átomo consistía dunha parte central moi pequena, que condensaba a carga positiva (núcleo), e dun conxunto de electróns que se movían dalgunha maneira a gran distancia, deixando un gran baleiro no medio. O modelo de Rutherford, moi suxestivo, estaba en desacordo coas concepcións da mecánica clásica e do electromagnetismo, e por iso N. Bohr en 1913, facendo unha síntese dos traballos de Planck e Rutherford, propuxo un modelo que, violando a electrodinámica clásica, conservaba o modelo mecánico clásico. Segundo Bohr, os electróns describían órbitas circulares, pero só aquelas nas que o momento angular era un múltiple íntegro positivo da constante de Planck. Non todas as órbitas eran posibles, senón só as permitidas pola anterior condición: as órbitas eran cuantizadas. Cando un electrón pasaba dunha das órbitas permitidas Eia outra Ejemitíase radiación de frecuencia v = |Ei- Ej|. Posteriores melloras do modelo, como a feita en 1915 por Sommerfeld, Wilson e Ishiwara ou a incorporación de aproximacións relativistas feita por Sommerfeld en 1919, conseguiron mellorar algún resultado, pero non acabaron de ter éxito. A solución chegou co nacemento da mecánica cuántica, obra de De Broglie, Heisenberg, Schrödinger e Born.
O átomo de hidróxeno segundo a mecánica cuántica
A mecánica cuántica dá lugar a un modelo bastante coidadoso do átomo máis sinxelo, o átomo de hidróxeno, que está formado só por un protón e un electrón. Foi resultado dun cambio conceptual profundo, no que as nocións básicas da mecánica clásica foron substituídas polas da mecánica cuántica: a información que se pode chegar a ter sobre o movemento dunha partícula é limitada; non se pode coñecer con precisión o valor de todas as variables. A función de onda é o concepto que vai substituír ao de traxectoria. As órbitas do modelo de Bohr deben ser substituídas por nubes de probabilidades que sinalan onde se pode atopar un electrón e onde non é moi posible. Estas zonas no contorno do núcleo son as solucións dunha ecuación dinámica (ecuación de Schrödinger). Os diferentes estados dos electróns forman os diferentes orbitais, concepto que substitúe ao das órbitas de Bohr.
Átomos polielectrónicos
Gracias a unha modificación do modelo cuántico do átomo de hidróxeno pódese ter unha idea da configuración electrónica dun átomo de número atómico Z. Neste caso a enerxía depende dos dous números cuánticos: n e l. Un electrón caracterízase por catro números cuánticos n, l, mle ms; ms número cuántico de spin, só pode ter os valores 1/2 ou -1/2. Os electróns deposítanse de forma progresiva nos sucesivos orbitais, atendendo ao principio de exclusión de Pauli. Para un mesmo valor de n, hai diferentes orbitais l, l=0,..., n-1. Os orbitais l denomínanse con letras: s(l=0), p(l=1), d(l=2), f(l=3). Un orbital s só pode ter dous electróns (ml=0, ms=91/2); e un p pode ter seis (ml=-1, 0, 1, ms=91/2); un d pode ter dez (ml=-2, -1, 0, 1, 2, ms=91/2). Da disposición dos electróns nestes orbitais resulta a configuración electrónica do elemento en cuestión. -
átomo mesónico
Átomo no que un electrón cortical foi substituído por un mesón. Como a masa dos mesóns é unhas duascentas veces maior cá do electrón, o radio de Bohr da órbita mesónica é unhas duascentas veces menor ca a do electrón, e a miúdo penetra no interior do núcleo.
-
átomo muónico
Átomo no que un electrón foi substituído por un muón.
-
s
m
-
s
m
Partícula moi pequena dunha cousa.
-
s
m
Cousa extremadamente pequena.
-
átomo social
[PSIC]
Estrutura das relacións entre o individuo e o seu grupo social, esquematizada en forma de atraccións e repulsións recíprocas. A representación gráfica do conxunto de átomos sociais dun grupo denomínase sociograma.