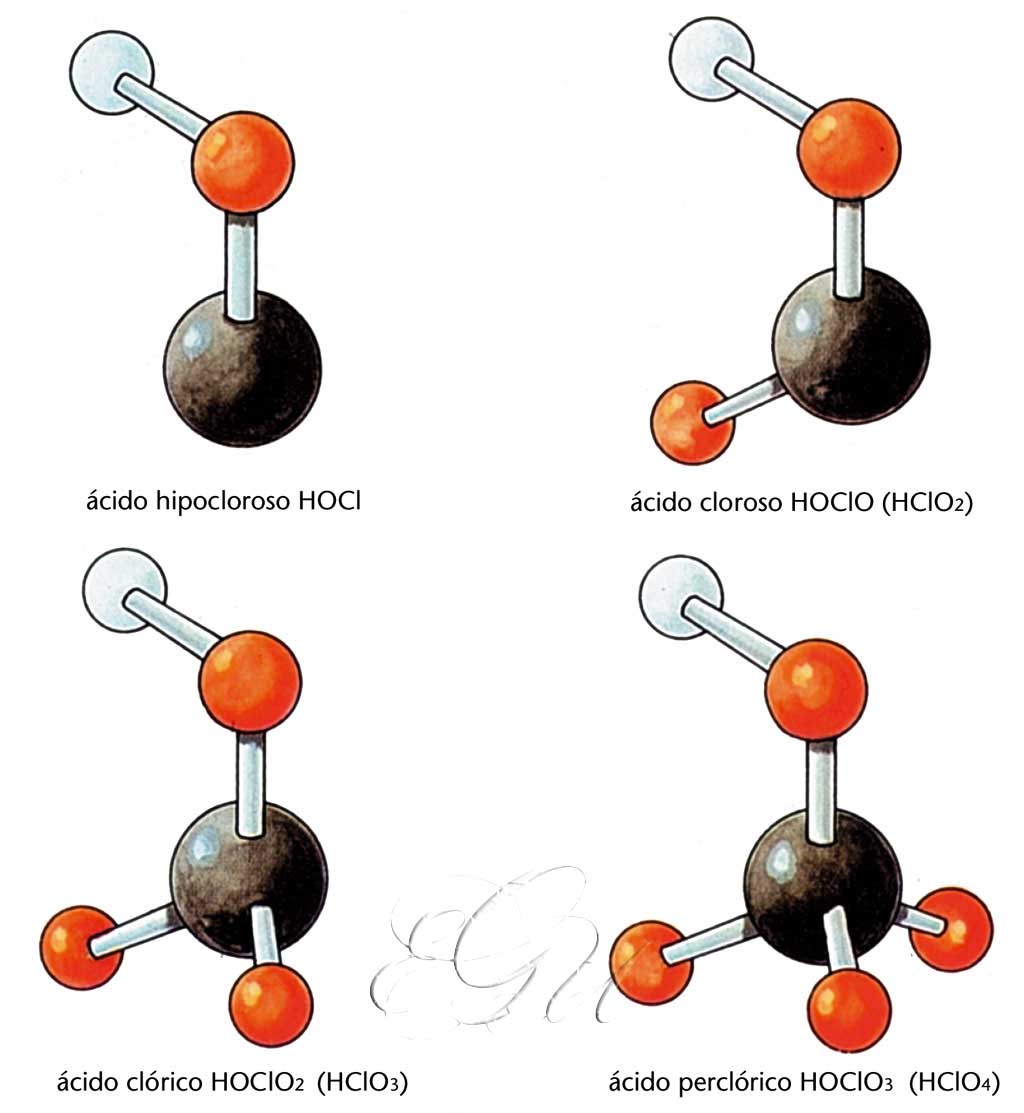
cloro
(
-
s
m
[QUÍM]
Elemento pertencente ao grupo VII da táboa periódica (grupo dos halóxenos), de número atómico 17 e peso atómico 35,453. O elemento natural é unha mestura dos núclidos 35 (75,4%) e 37 (24,6%); tamén se lle coñecen os isótopos artificiais 32, 33, 34, 36, 38, 39 e 40. É un gas diatómico tóxico de cor verde. En 1646 J. R. Glauber describiu a preparación e en 1772 J. Priestley foi o primeiro en obter a forma anhidra; poucos anos despois, en 1774, K. W. Schelee obtívoo por oxidación do ácido clorhídrico. A codia terrestre ten un 0,2 % de cloro na súa composición, e a auga do mar ten unha proporción de 2,5 % en forma de cloruro de sodio. En estado natural existe en forma de cloruros cristalizados, dos que os máis coñecidos son: cloruro de sodio, sal xema ou hialita, silvina, silvinita e carnalita, todos activamente explotados. De cheiro forte e sufocante, o cloro é un tóxico activo que provoca a morte en poucos minutos se o aire respirado contén máis de 2,5 mg/l; foi o primeiro gas asfixiante empregado na Primeira Guerra Mundial. O cloro dá dous tipos de enlace: o enlace covalente simple, con el mesmo, compartindo un par de electróns, e o enlace iónico, cando se combina cun átomo feblemente electronegativo. O seu grao de oxidación normal é -1 (ión Cl - ), pero pode presentar graos +1, +3, +4, +5 e +7. O cloro é un corpo moi activo que se combina directamente con todos os elementos, agás os gases nobres, o osíxeno, o nitróxeno e o carbono. Ataca todos os metais, moitas veces con incandescencia, e a presencia de vapor de auga intensifica notablemente a reacción. Reacciona cos elementos metálicos e non metálicos para dar cloruros. Destrúe tamén todos os compostos hidroxenados e metálicos non osixenados, agás o fluoruro de hidróxeno (H 2 F 2 ). Os hidrocarburos inflámanse, as máis das veces espontaneamente, nunha atmosfera de cloro; tamén se observan reaccións de fixación do cloro sobre enlaces triples (CHºCH+Cl 2 →CHCl=CHCl) e dobres (CH 2 =CH 2 +Cl 2 → CH 2 Cl-CH 2 Cl) ou de substitución: CH 4 +Cl 2 →CH 3 Cl. A acción do cloro sobre os compostos hidroxenados ou metálicos que conteñen osíxeno conduce en xeral a un equilibrio con formación dun cloruro, cando se trata do óxido metálico correspondente ao grao de oxidación máis estable ou, ás veces, dun oxicloruro. O cloro gasoso combínase co vapor de auga segundo a reacción H 2 O+Cl 2 →2HCl+1/2O 2 ; coa auga dá a auga de cloro. En presenza de hidróxido de sodio (sosa cáustica) a reacción é total: Cl 2 +2(Na + OH - )→ Na + Cl - +Na + ClO+H 2 O, de onde se obtén a lixivia, utilizada como decolorante e bactericida, propiedades debidas ao hipoclorito de sodio, que se descompón cunha gran facilidade: Na + ClO - →Na + Cl - +1/2O 2 . O cloro úsase como decolorante, como bactericida, no branqueo de materias vexetais e para a fabricación de cloruros decolorantes. A industria química consome unha proporción moi importante para a obtención de produtos acabados, ou intermediarios, indispensables para facer a síntese de produtos de gran consumo, como o tetracloruro de carbono, empregado como solvente líquido de extintores; o cloruro de xofre, usado na vulcanización do caucho; o cloroformo, solvente; o cloruro de metano, refrixerante e anestésico local; o diclorodifluorometano, líquido refrixerante; o DDT ou diclorodifeniltricloretano, insecticida, etc.
-
cloro residual
[QUÍM]
Cantidade de cloro que queda presente na auga con actividade bactericida. No fornecemento de auga ás poboacións ten que ser da orde de 0,2 a 0,5 mg/l a fin de asegurar a súa potabilidade durante o paso pola rede de distribución.