solución
(< lat solutĭōne)
-
[QUÍM]
-
s
f
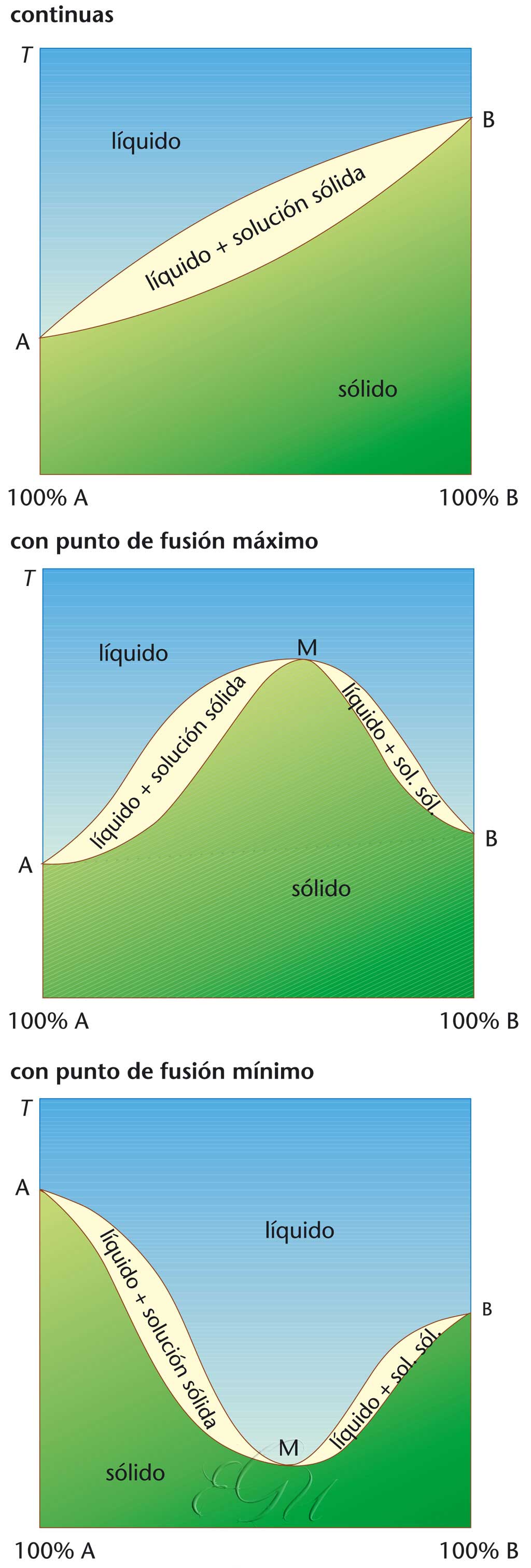
Mestura en que os compoñentes se distribúen homoxeneamente en toda a extensión do sistema. Nos sistemas binarios, adoita denominarse soluto o compoñente minoritario, e disolvente ao maioritario, clasificación que se pode estender aos sistemas de máis compoñentes. En función do estado físico en que teñen lugar, distínguense as solucións sólidas, líquidas e gasosas. As solucións sólidas fórmanse mediante a interpenetración das redes cristalinas dos compoñentes e a súa formación esixe a existencia de estruturas cristalinas idénticas. Os seus compoñentes poden ser parcial ou totalmente miscibles; neste último caso, desde un punto de vista termodinámico e segundo as curvas do equilibrio sólido-líquido, pódense clasificar en solución sólidas continuas, cun punto de fusión que evoluciona proporcionalmente á concentración dos compoñentes; solucións sólidas con punto de fusión máximo, que son máis ben raras; e as solucións sólidas con punto de fusión mínimo que teñen lugar con gran frecuencia e das que son exemplos diversos sistemas metálicos, en particular as aliaxes fusibles. Nas solucións sólidas con compoñentes parcialmente miscibles, os límites de concentración entre os que existe a solución dependen da temperatura, de maneira que poden existir dúas solucións sólidas conxugadas, de forma semellante ao que ocorre entre líquidos parcialmente miscibles. Desde un punto de vista termodinámico e segundo as súas curvas de equilibrio sólido-líquido, as solucións deste tipo poden presentar un punto eutéctico, como ocorre no sistema ouro-níquel, ou un punto peritéctico, como ocorre no sistema cadmio-mercurio. Polo que respecta aos gases, estes presentan unha miscibilidade total, e non hai nas solucións gasosas ningún tipo de interacción interatómica ou intermolecular importante, de maneira que, en condicións ideais, obedecen á lei das presións de Dalton. Porén, nos sistemas gasosos reais cómpre substituír a variable de estado presión parcial pola fugacidade. As solucións líquidas , clasifícanse, segundo cumpran ou non a lei de Raoult, en ideais e non ideais ou reais. Existen, en cambio, moi poucas solucións ideais para cada un dos seus compoñentes no intervalo completo de concentracións. A gran maioría de solucións líquidas presentan, polo tanto, desviacións á lei de Raoult, e poden ser tanto positivas coma negativas. Por outra banda, as solucións líquidas clasifícanse en diluídas e concentradas, segundo un compoñente estea ou non en en exceso respecto do outro. Desde o punto de vista da natureza química do soluto, distínguense as solucións moleculares, en que as moléculas de soluto existen como tales e provocan a variación prevista nas propiedades coligativas, e as solucións iónicas, en que o soluto (electrólito) se atopa totalmente ou parcialmente disociado en entidades iónicas, cousa coa que se orixinan variacións excesivas nas propiedades coligativas. Neste tipo de solución o concepto de concentración substitúese polos de actividade e coeficiente de actividade, mentres que existen como medida de concentración a forza iónica.
Sinónimos: disolución. -
solución hipertónica
Solución que ten unha presión osmótica superior ca a outra disolución de referencia. OBS: Tamén se denomina solución hiperosmótica.
-
s
f
-
s
f
-
Acción de resolver un problema ou unha cuestión.
-
Aquilo que resolve un problema ou unha cuestión.
-
[MAT]
resultado.
-
-
solución de continuidade
-
Interrupción nunha continuidade dunha cousa.
-
Separación, división ou dislocación de partes continuas, como é o caso, por exemplo da fractura dun óso.
-
Refráns
- Cun lobo non se mata outro.