carbono
(< carbón)
-
s
m
[QUÍM/BIOL]
Elemento non metálico pertencente ao grupo IV da táboa periódica, de peso atómico 12,011 e número atómico 6. O carbono terrestre componse dos núclidos 12 (98,9%) e 13 (1,1%), e do gas carbónico atmosférico (CO 2 ); contén, ademais, unha pequena pero constante porcentaxe de carbono 14 (isótopo radioactivo). Este núclido radiactivo natural ten unha vida media de 5.580 anos. Fórmase continuamente na atmosfera pola acción dos neutróns que proveñen dos raios cósmicos sobre o nitróxeno: 14 7 N+ 1 0 n → 14 6 C+ 1 1 p, e a súa desintegración prodúcese segundo a reacción: 14 6 C → 14 7 N+ -0 1 e. Ademais, como as reaccións se producen á mesma velocidade, a proporción de carbono 14, dentro do dióxido de carbono atmosférico, mantense constante. As plantas absorben por fotosíntese o gas carbónico atmosférico; polo que os seus hidratos de carbono conteñen os núclidos 12 e 14 en proporción constante mentres as plantas están vivas. Cando morren, a proporción de carbono 14/carbono 12 diminúe por desintegración do núclido 14. Neste feito baséase a técnica de datación absoluta empregada en arqueoloxía. O carbono 14 úsase tamén como trazador radioactivo para esclarecer o mecanismo de certas reaccións orgánicas complexas. Tamén se coñecen os núclidos artificiais 10, 11 e 15. O peso atómico do núclido 12 escolleuse como base do sistema internacional de pesos ou masas atómicas. O carbono constitúe o 0,2% da codia terrestre e resulta raro atopalo nas rochas eruptivas, se ben abunda nas sedimentarias, nos xacementos de combustibles sólidos e líquidos (hulla e hidrocarburos) e nos depósitos de carbonatos. Tamén existe, baixo a forma de dióxido de carbono, na atmosfera e nas augas naturais. O 90% dos compostos químicos coñecidos son substancias orgánicas que conteñen carbono, feito que indica o claro predominio deste elemento na materia viva, resultado da súa versatilidade química se se compara con todos os demais elementos. O carbono posúe a propiedade singular de formar un número virtualmente infinito de compostos como resultado da súa capacidade de establecer ata catro enlaces covalentes moi estables, dirixidos cara aos vértices dun hipotético tetraedro. Posúe catro electróns na súa capa máis externa e polo tanto a posibilidade de unirse a outros elementos ou a outros átomos similares; por medio de enlaces sinxelos, dobres ou triples, orixina estruturas complexas, como cadeas lineais ou ramificadas e aneis, de grande importancia biolóxica. Ademais, introduce conformacións tridimensionais nas moléculas, de moita importancia para a realización de funcións nos seres vivos. O carbono encóntrase na natureza baixo dúas formas alotrópicas, o diamante e o grafito e baixo unha serie de variedades amorfas como a antracita, a hulla, o lignito e a turba. Todos eles son o resultado dos cambios graduais que sofre a materia orgánica vexetal pola acción física do enterramento prolongado, do progresivo aumento da presión e da temperatura en profundidade e da acción química de bacterias anaeróbicas. Outra forma amorfa é a de orixe vexetal, que se obtén por quentamento da madeira en ausencia de aire. O cristal de grafito é plano e romboédrico, cos átomos de carbono ordenados nunha distribución hexagonal e cunha densidade de 2,26 g/cm 3 . Cada carbono está unido a outros tres mediante dous enlaces sinxelos e un enlace dobre, mentres que as forzas entre as capas de átomos son débiles; deste xeito, cando se emprega un lapis de grafito deposítanse sobre o soporte finas capas deste mineral. No diamante cada carbono forma catro enlaces sinxelos con outros catro átomos de carbono de forma que, distribuídos tetraedricamente, constitúen unha rede tridemensional moi forte, cunha densidade de 3,51 g/cm 3 , que lle confire ao diamante unha das maiores durezas dentro dos minerais. A conversión de grafito en diamante conséguese a 2.000°C e 100.000 atm; os científicos de General Electric levárona a cabo por vez primeira en 1954 e obtiveron os primeiros diamantes sintéticos. Por isto, a maior parte dos diamantes empregados de xeito industrial, para cortar ou moer, teñen esta mesma orixe. Os grafitos artificiais son materiais duros e resistentes que se utilizan na fabricación de electrodos, crisois, resistencias eléctricas, etc; a variedade pirolítica ou pirografítica, dunha anisotropía remarcable, ten unha gran condutividade térmica e eléctrica e é moi resistente á oxidación. A situación do carbono no eixe da táboa periódica, a medio camiño entre os elementos máis electropositivos e os máis electronegativos, explica a variedade dos corpos que permite formar e o gran número de reaccións nas que participa. O átomo de carbono posúe catro electróns de valencia na capa L e, xa que tanto a formación do catión C 4+ como a do anión C 4- son enerxeticamente moi desfavorables, únese aos outros elementos formando enlaces covalentes ou coordinados. O átomo de carbono represéntase dende o s XIX mediante un tetraedro regular e a cada un dos seus vértices diríxese unha valencia; esta estrutura explicouse posteriormente por medio da teoría da hibridación dos orbitais. As propiedades químicas do carbono son comúns a todas as súas formas alotrópicas, pero estas reaccionan a velocidades distintas. O carbono únese ao hidróxeno a temperaturas moi elevadas dando acetileno e, a temperaturas máis baixas, reversiblemente, metano. Únense a numerosos metais a temperatura do forno eléctrico para dar carburos. O carbono, actuando como elemento electropositivo, combínase co fluor e dá tetrafluoruro de carbono (CF 4 ), pero non cos outros halóxenos. Inflámase en atmosfera de osíxeno ou aire cando se leva a unha certa temperatura inicial que depende da variedade alotrópica: 800-850°C para o diamante, 700°C para o grafito e 350°C para o carbono amorfo. A combustión do carbono en exceso de aire non produce temperaturas superiores a 500°C e conduce á formación de dióxido de carbono, unicamente, nunha reacción fortemente exotérmica (?H=393kJ/mol): C+O 2 →CO 2 . A unha temperatura superior a 1.000°C, a combustión produce óxido de carbono: 2C+O 2 →2CO (?H= -220 kJ). A temperaturas entre 500 e 1.000°C os gases que se obteñen son unha mestura dos dous óxidos e, canto máis elevada é a temperatura, maior é a proporción de monóxido. O carbono posúe propiedades redutoras importantes; o vapor de auga redúcese polo coque incandescente (1.000°C) segundo a reacción C+H 2 O→CO+H 2 (?H=130 kJ), e a mestura de gases resultante utilízase como combustible. Se a temperatura non é tan alta, prodúcese a reacción C+2H 2 O→CO 2 +2H 2 (?H=84kJ) e obtense un gas combustible menos rico en calorías. En ausencia de osíxeno, o carbono reduce case todos os óxidos metálicos a metal; a temperatura necesaria para levar a cabo a reacción é tan elevada como estable se mantén o óxido. O carbono reduce tamén facilmente os ácidos e os sales osixenados. Así, o ácido fosforoso e o anhídrido fosfórico redúcense a 1.000°C e a reacción utilízase para a obtención do fósforo. A redución dos nitratos, dos cloratos e, sobre todo, dos percloratos dá lugar a reaccións explosivas, propiedade utilizada para a fabricación da pólvora ordinaria. Á temperatura do arco eléctrico, o carbono únese ao nitróxeno e obtense cianóxeno: 2C+N 2 →C 2 N 2 (?H=305kJ); en presenza de hidróxeno prodúcese cianuro de hidróxeno: C 2 N 2 +H 2 →2HCN (?H= -46kJ). O silicio e o boro liberan directamente carburos (SiC e B 4 C). O carbono dá co hidróxeno un número extremadamente elevado de compostos e o estudo destes compostos constitúe o obxecto da química orgánica. O carácter único do carbono neste sentido provén da solidez dos enlaces entre os seus propios átomos (enlaces C-C), fortes incluso cando os átomos de carbono van ligados a outros elementos, a diferenza do que ocorre co boro, o silicio, o fósforo, etc, xa que a partir deles non se poden preparar compostos estables análogos aos de carbono. A propiedade que ten o carbono de establecer enlaces covalentes (simples, dobres ou triples) con outros átomos do mesmo elemento ou con elementos diferentes, como o nitróxeno, permítelle constituír cadeas de lonxitudes e disposicións espaciais variadísimas. Estas estruturas tan singulares son, de feito, as únicas capaces de incluír toda a complexidade e diversidade necesarias para desenvolver as reaccións químicas propias dos organismos vivos (intercambios de enerxía, almacenamento de información, función plástica, etc). Por este motivo, aínda que é un elemento raro no cosmos (0,15%), os seres vivos coñecidos souberon concentralo e incorporalo ao seu organismo (10-19% por termo medio). O carbono, que estaba presente na súa maior parte como CO 2 na atmosfera primitiva, disolveuse rapidamente na hidrosfera, onde pasou tamén ás formas de ión bicarbonato e de ión carbonato. Esta reserva actuou, dende aquela, como factor estabilizador de primeira magnitude do CO 2 atmosférico. A actividade dos organismos fotosintetizadores fixou unha parte do carbono en forma de materia orgánica e carbonatos, e o osíxeno restante enriqueceu a composición do aire. Así, a proporción de CO 2 na atmosfera diminuíu de tal xeito que agora a maior parte do carbono está inmobilizado en forma de sedimentos organóxenos (sobre todo carbonatos e materia orgánica fósil). A proporción actual de CO 2 na atmosfera tende a aumentar, por efecto da combustión de carbóns e de petróleo, da calcinación dos carbonatos, etc. No mar, ademais do carbono presente nos seres vivos, está o carbono da materia orgánica morta en forma de partículas en suspensión e o da materia orgánica disolta. Na litosfera o carbono acumúlase nas plantas lignificadas dos bosques e na materia orgánica do solo.
-
carbono 12/13
[ARQUEOL]
Técnica de análise realizada sobre mostras de coláxeno humano para estudar a dieta alimenticia e mostrar a importancia relativa que o consumo cárnico ou de vexetais tiña nos grupos humanos prehistóricos. O fundamento deste procedemento analítico é o diferente contido que os animais e plantas consumidos teñen do isótopo carbono 13, que queda fixado no coláxeno humano.
-
carbono 14
[ARQUEOL]
Método de datación absoluta baseado na radioactividade atómica do carbono proposto por W. Libby (1950) que permitiu datar a morte dos seres vivos e obter, por vez primeira, datas absolutas válidas para determinados períodos da Prehistoria, o que facilitou unha mellor valoración da cronoloxía prehistórica. As datacións do carbono 14, sen embargo, teñen un límite temporal situado ao redor de 40.000/50.000 BP (Musteriense) debido a que para datas maiores a proporción de radiación adoita ser demasiado pequena para ser medida con fiabilidade. Este método resulta especialmente útil desde o Paleolítico superior ata o Bronce ou Ferro, xa que a partir desas épocas os sistemas tradicionais de datación histórica son, polo xeral, máis precisos ca o carbono 14. Utilízase tamén para materiais posteriores, procedentes de territorios xeralmente non europeos, que non teñen posibilidades cronolóxicas derivadas dos métodos arqueolóxicos. Os laboratorios proporcionan a data media Before Present (BP ‘antes do presente’) e o erro típico, como por exemplo 3650±100 BP, data do campaniforme das Pontes de García Rodríguez. A interpretación correcta da data debe realizarse tendo en conta as seguintes precaucións: a data BP convértese nunha data do calendario gregoriano restando 1950 (ano que por convención se considera “presente”), polo que pasa a ser o 1700 a C. Ademais, diversos factores de tipo aleatorio fan que se obteña unha data probable acoutada por un intervalo de variación estatística que, segundo a curva normal de Gauss, ofrece a porcentaxe de que a data real estea alí contida. Seguindo o exemplo anterior, débese interpretar que a probabilidade de que a data real estea entre 1600 e 1800 a C (sumando e restando unha vez o erro típico) é do 68%, e entre 1500 e 1900 a C (dúas veces o erro) do 95%. O problema maior do método débese a que o carbono 14 que existe na actualidade non coincide exactamente co que había no momento en que estaba vivo o organismo analizado, polo que se producen máis erros canto máis antigo sexa o material: ata o 2000 a C as datas poden ser uns séculos máis antigas, pero canto máis se retroceda no tempo, o erro pode superar o milenio. Para evitar este inconveniente os laboratorios ofrecen datas calibradas mediante curvas ou táboas establecidas por comparación entre as datas ofrecidas polo carbono 14 coas obtidas pola dendrocronoloxía para unha mesma madeira.
-
carbono asimétrico
[QUÍM]
Átomo de carbono enlazado a catro átomos ou grupos diferentes. Un átomo de carbono asimétrico confire unha disimetría á molécula que o contén e, como consecuencia, esta molécula presenta actividade óptica. A distribución diferente dos catro substituíntes do carbono asimétrico (formando dúas moléculas con configuracións que teñan a mesma relación que hai entre un obxecto e a súa imaxe nun espello) dá lugar á existencia de dous isómeros opticamente activos.
-
ciclo do carbono
[BIOL]
-
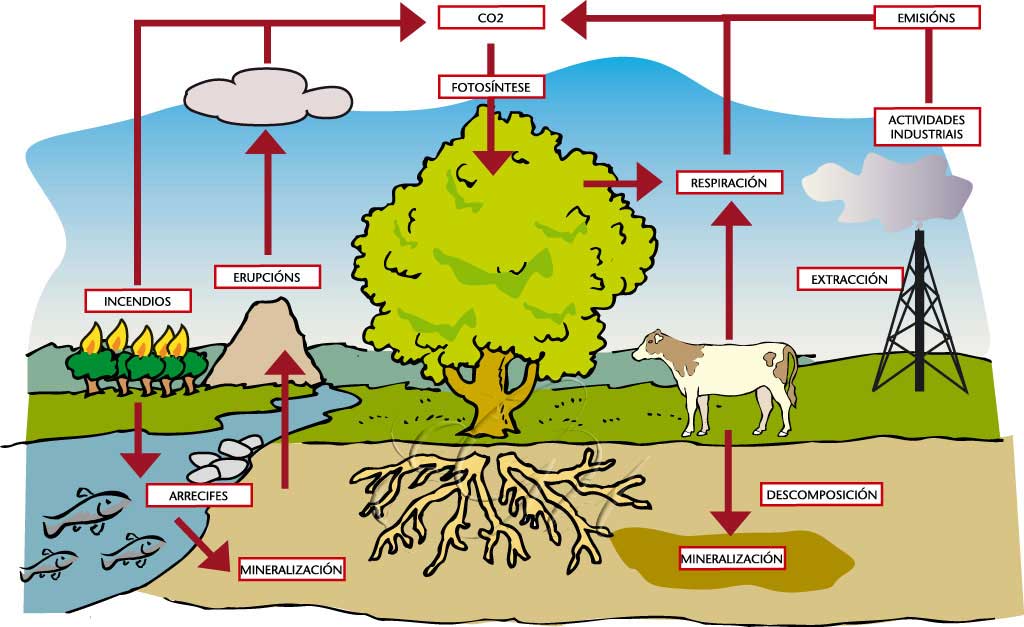
Conxunto de estadios polos que pasa o carbono ao longo do proceso pechado ao que se somete pola acción dos seres vivos. A significación biolóxica deste ciclo é moi importante, xa que sinala, en liñas xerais, os sistemas de aproveitamento da enerxía por parte da biosfera, enerxía que conteñen os compostos máis ou menos reducidos de carbono, así como a súa utilización como material constitutivo dos seres vivos. O carbono, procedente do dióxido de carbono do aire, da auga ou do bicarbonato da auga, entra nos seres vivos autotróficos (produtores primarios) grazas a reaccións de síntese (fotosíntese, quimiosíntese). Os mesmos organismos oxidan unha boa parte da materia orgánica sintetizada. Do resto, unha parte libérase ao medio e a outra vólvese constitutiva do organismo sintetizador e adoita incorporarse aos organismos heterotróficos. Finalmente, toda a materia mineralízase ben en vida dos organismos que a absorberan ou grazas á actividade de axentes como bacterias ou fungos, entre outros, que descompoñen os cadáveres, os excrementos, etc. Polo tanto, en último termo, o carbono volve formar dióxido de carbono, pasa ao aire ou á auga e péchase o ciclo, que é bastante rápido. Pode quedar unha parte do carbono inmobilizada no solo (ácidos húmicos) ou nos sedimentos de nova formación (cunchas, ósos, etc), que dan lugar á formación de rochas carbonadas organóxenas. Pese a que neste caso é máis lento, pódese chegar tamén a pechar o ciclo por redisolución dos carbonatos, metamorfismo, vulcanismo, combustión do carbón ou do petróleo.
-
Conxunto de procesos bioquímicos realizados polos organismos fotosintéticos durante a fase escura da fotosíntese, na que o carbono inorgánico en forma de CO 2 pasa a formar parte de diversos glícidos por redución.
-
-
dióxido de carbono
[QUÍM]
Gas incoloro que ten un olor picante e sabor ácido, bastante soluble en auga, produto da combustión do carbón e da materia orgánica en exceso de osíxeno, descuberto por J. B. van Helmont (1630) e analizado por A. L. Lavoisier (1783). Está presente na atmosfera, nunha proporción sensiblemente constante do 0,03% en volume, malia as transformacións ás que se ve sometido, como a fotosíntese e a respiración. Localízase nos gases volcánicos, en mesturas gasosas de minas de hulla e disolto a presión en numerosas augas minerais, das que se desprende cando chega ao aire libre. Obtense industrialmente como subprodutor en diversas industrias: síntese do amoníaco, fermentación alcohólica dos azucres, fabricación do cal e dos cementos, etc; sepárase dos gases cos que está mesturado por disolución en auga a presión e despois descomprímese a solución. No laboratorio pódese producir por descomposición térmica do bicarbonato de sodio: 2NaHCO 3 →Na 2 CO 3 +H 2 O+CO 2 . A súa densidade respecto ao aire é de 1,53; a temperatura crítica, 31,1°C; a presión crítica, 7,3 MPa; e o seu punto tripla corresponde a unha presión de 0,5 MPa. Solidifica directamente ao arrefrialo a -78,5°C. Por razóns aínda non moi ben coñecidas, sen ser tóxico impide a respiración por algunha acción situada a nivel da parede pulmonar. É un gas moi estable, que só se disocia a temperaturas superiores a 1.300°C. O carbono e o hidróxeno fan que o CO 2 se reduza a CO, pero algúns metais redutores fan que se reduza a carbono elemental. As súas solucións en auga son pouco ácidas (auga carbónica). Utilízase como fluído de refrixeración e como intermediario químico para obter atmosferas inertes en extintores de incendios e en aerosois. Utilízase tamén como materia prima na fabricación da sosa polo procedemento de Solvay, na industria azucreira e na preparación de augas e bebidas carbónicas. O dióxido de carbono intervén no mantemento do pH sanguíneo. Constitúe, baixo a forma de bicarbonato sódico, a reserva alcalina, e é un importante factor regulador da ventilación pulmonar. Unicamente se elimina unha parte do CO 2 metabolizado nos pulmóns durante a expiración. O CO 2 sanguíneo, procedente dos tecidos, está disolto en forma de ácido carbónico, unido á hemoglobina e en forma de ión bicarbonato. A hemoglobina intervén tamén indirectamente no transporte de CO 2 . A anhidrase carbónica, un enzima presente nos eritrocitos, acelera notablemente a liberación de CO 2 a partir do ión bicarbonato. Unha excesiva eliminacion de CO 2 no curso dunha hiperpnea orixina unha alcalose. OBS: O dióxido de carbono tamén se coñece baixo as denominacións de anhídrido carbónico e gas carbónico.
-
disulfuro de carbono
[QUÍM]
Líquido inflamable de olor etéreo; o produto comercial ten un olor desagradable a causa da presenza de impurezas sulfuradas. Descuberto por Lampadius en 1796, obtense actualmente por síntese directa como consecuencia da acción do vapor de xofre sobre coque: C+S 2 → CS 2 (?H=-50kJ). Ferve a 46,5°C, o seu punto de inflamación é -30°C e forma co aire mesturas detonantes. Úsase na vulcanización do caucho en frío, na manufactura do raión, do celofán, do tetracloruro de carbono, como axente de flotación e tamén como disolvente de graxas, resinas e gomas.
-
fibra de carbono
[TECNOL/QUÍM]
Filamentos de carbono que se utilizan na fabricación de materiais compostos, co fin de darlles lixeireza ademais de rixidez e resistencia. As fibras de carbono obtéñense mediante o quentamento dos filamentos dun material que contén carbono ata que desaparecen todos os elementos agás el, momento en que se embebe nunha matriz de resinas. Fabrícanse, polo xeral, a partir de fibras celulósicas ou de fibras acrílicas, mesmo de brea de hulla ou de polímeros termicamente estables. Polas propiedades térmicas, mecánicas e de fricción que presentan, ademais da súa baixa densidade, utilízanse especialmente na industria aeronáutica, na automobilística e na fabricación de artigos deportivos.
-
ión carbono
[QUÍM]
Catión orgánico no que o defecto de carga electrónica se localiza nun átomo de carbono. Os ións carbono son electrófilos e posúen unha gran reactividade de cara aos reactivos que poidan subministrar pares de electróns e formar con eles un enlace covalente. Son especies de existencia transitoria dentro do curso dunha reacción e tenden a unirse co catalizador presente ou a autoestabilizarse por atracción dun par de electróns dun átomo de carbono ou dun grupo adxacente formando un dobre enlace. A súa estabilidade depende en último termo da posibilidade de repartición da carga positiva do átomo de carbono sobre os átomos adxacentes. Deste xeito, a estabilidade dos ións alquilo-carbono de estrutura simple medra ao aumentar a súa substitución: CH 3 < RCH 2 <RRCH<RRRC. Ademais de intervir nas reaccións de substitución nucleófila, os ións carbono tamén interveñen en reaccións de eliminación dun protón e sobre todo noutras de reorganización estrutural, como a transposición de Wolff e a transposición alílica. Os ións carbono desempeñan un papel importante en moitas reaccións de interese práctico como as de hidroxenación, deshidroxenación, alquilación e outras, empregadas en petroleoquímica para a obtención de carburantes e outros produtos.
-
monóxido de carbono
[QUÍM]
Gas incoloro, tóxico, descuberto por Joseph Priestley (1772) e estudado por Humphry Davy (1808). É o produto resultante da oxidación incompleta do carbono polo osíxeno; tamén é o constituínte combustible de diferentes mesturas gasosas industriais e o redutor gasoso máis utilizado en metalurxia. Prepárase industrialmente por combustión do carbón con aire en defecto. No laboratorio obtense puro por deshidratación do ácido fórmico: HCOOH→ CO 2 +H 2 O. A súa estrutura molecular aínda se discute, aínda que se acepta a seguinte: C=O, que manifesta a presenza de dúas covalencias normais e unha covalencia dativa, cos dous electróns fornecidos polo osíxeno. O monóxido de carbono é sumamente tóxico para todos os vertebrados a causa da formación de carboxihemoglobina, que impide a función normal da hemoglobina do sangue. Como ten un peso específico moi semellante ao do aire, difúndese moi ben nel, de xeito que aumenta o perigo de envelenamento. É, esencialmente, un composto non saturado no que o carbono tende a recuperar o seu grao de oxidación normal (4) e é, xa que logo, redutor: cos halóxenos dá haloxenuros de carbonilo COX 2 , co xofre dá COS e co osíxeno, CO 2 . O monóxido de carbono reduce un gran número de óxidos metálicos: algúns de metais nobres (como o paladio, a prata e o ouro) redúcense incluso a temperatura ordinaria; pola contra, os metais moi oxidables (MgO,Al 2 O 3 ) non se poden reducir nos límites das temperaturas realizables industrialmente. En auga ten lugar a reacción reversible CO+H 2 O →CO 2 +H 2 (?H=-42kJ). O monóxido de carbono reacciona tamén como oxidante cos metais alcalinos, pero as reaccións máis importantes industrialmente son as do hidróxeno, co que dá produtos totalmente diferentes segundo a temperatura e a presión aplicadas e a natureza do catalizador utilizado. OBS: Tamén se coñece coa denominación de óxido de carbono.
-
oxicloruro de carbono
[QUÍM]
fosxeno.
-
subóxido de carbono
[QUÍM]
-
Cada un dos óxidos de carbono que conteñen unha relación de átomos de osíxeno respecto a átomos de carbono inferior a 1.
-
Denominación non sistemática do dióxido de tricarbono, de fórmula empírica C 3 O 2 H que corresponde á estrutural O=C=C=C=O. Obtense por deshidratación do malonato de etilo ou do ácido malónico cun exceso de anhídrido fosfórico a 300°C. En condicións ambientais é un gas incoloro que ten como punto de fusión -111°C e como punto de ebulición +6°C. É pouco estable e descomponse a 200°C segundo a reacción C 3 O 2 →CO 2 +2C graf . A temperatura ordinaria, o subóxido de carbono polimeriza e orixina un sólido vermello, soluble en auga, de composición non definida.
-
-
sulfuro de carbono
[QUÍM]
Cada un dos compostos binarios de xofre e carbono. Coñécense tres que se corresponden cos tres óxidos principais: o monosulfuro (CS), sólido que probablemente só existe en estado polimerizado; o subsulfuro (C 3 S 2 ), líquido lacrimóxeno; e o disulfuro (CS 2 ), chamado propiamente sulfuro de carbono, que actúa de forma lixeira como anestésico local e parasiticida.
-
tetracloruro de carbono
[QUÍM]
Líquido de olor semellante ao do cloroformo, con punto de ebulición 76,7°C, punto de fusión 22,9°C e peso específico 1,6 g/ml. Obtense industrialmente pola acción do cloro ou do cloruro de xofre sobre o sulfuro de carbono, en presenza dun catalizador (cloruro de antimonio ou cloruro de aluminio): 2Cl 2 +CS 2 →CCl 4 +2S; 2S 2 Cl 2 +CS 2 → CCl 4 +6S. É insoluble en auga, bo disolvente das materias graxas e utilízase como disolvente e como produto extintor. Combínase co trióxido de xofre con formación de fosxeno e de cloruro de pirosulfonilo: 2SO 3 +CCl 4 → COCl 2 +S 2 O 5 Cl 2 . En medicina utilízase como antihelmíntico.