nitróxeno
(
-
-
s
m
[QUÍM]
Elemento químico non metálico que pertence ao grupo V A da táboa periódica e que está situado entre o carbono e o osíxeno. É un gas incoloro, inodoro e insípido, e o elemento máis lixeiro do grupo. Descubriuno D. Rutherford en 1772, e na mesma época, tamén H. Cavendish e J. Priestley. En estado natural o nitróxeno molecular, a temperatura ambiente, é un gas que constitúe unha gran parte da atmosfera. En estado combinado é un dos principais constituíntes das proteínas animais e vexetais e dun gran número de substancias orgánicas. O nitrato de Chile é o principal mineral que contén nitróxeno combinado. A estrutura electrónico-molecular do nitróxeno é [N≣N], onde presenta un triplo enlace covalente. O nitróxeno diferénciase dos elementos do seu grupo por tres caracteres importantes: en primeiro lugar, non pode ter máis de oito electróns na súa capa externa, e polo tanto non pode formar máis de catro enlaces dirixidos que segue o orbital s e tres orbitais p. En segundo lugar, o nitróxeno forma facilmente dobres e triplos enlaces, mentres que no caso dos outros membros da familia a tendencia é menos clara, razón pola que os dobres enlaces son abondosos na química do nitróxeno. En terceiro lugar, a pequena dimensión do átomo de nitróxeno limita o seu número de coordinación, por impedimento estérico. Os cambios de fase son determinados polo nitróxeno molecular á presión atmosférica:
FORMULA
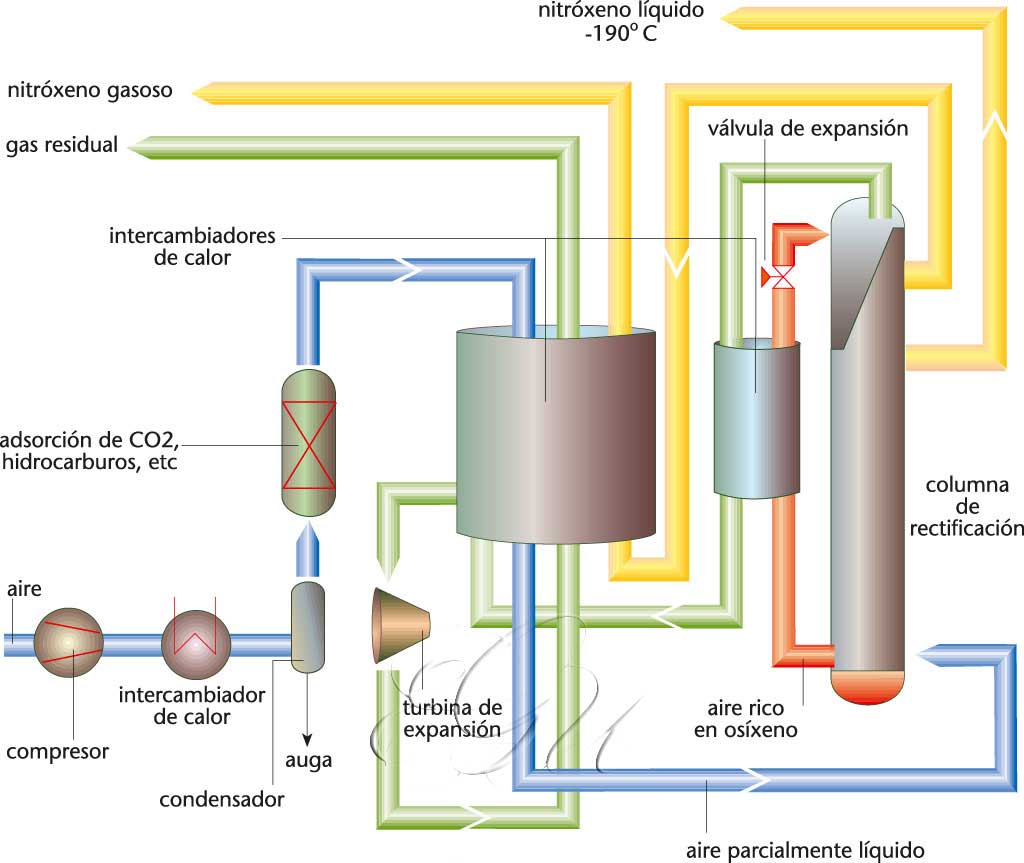
O nitróxeno obtense no laboratorio mediante a reacción NaNO2 + NH4Cl D N2 l + NaCl + 2H2O, e tamén por oxidación do amoníaco (NH3+ HNO2D 2H2O + N2l). Industrialmente, obtense por destilación fraccionada a baixa temperatura do aire líquido. O nitróxeno elemental non reacciona a temperatura ambiente coa maioría das substancias. A alta temperatura, a forma molecular reacciona con metais como o cromo, o silicio, o titanio, o aluminio, o boro, o berilio, o magnesio, o bario, o estroncio, o calcio e o litio, e forma nitruros, segundo a reacción 3Ca+N2D Ca3N2. Co osíxeno, a alta temperatura (2.000 a 3.000°C), forma NO, e co hidróxeno, forma o amoníaco a baixa temperatura e a alta presión, en presenza de catalizadores. O nitróxeno en estado puro emprégase moito como materia base para a preparación de compostos, como o amoníaco, os sales de amonio, o ácido nítrico e os nitratos, a urea e a cianamida de calcio. As propiedades crioxénicas empréganse na conservación de alimentos conxelados e tamén en medicina, grazas á posibilidade de conservar órganos enteiros durante un longo período de tempo. -
dióxido de nitróxeno [NO 2 ]
[QUÍM]
Líquido que se atopa en equilibrio co tetróxido de dinitróxeno (N 2 O 4 ä 2NO 2 ) que depende da temperatura e do estado físico. Pode obterse por descomposición do nitrato de chumbo segundo a reacción Pb(NO 3 ) 2 D PbO + 2NO 2 + O 2 e emprégase, debido a que é un axente oxidante, nas cámaras de chumbo para a obtención do ácido sulfúrico.
-
monóxido de nitróxeno [NO]
[QUÍM]
Gas incoloro, cun punto de ebulición de -151,8°C e un punto de fusión de -163°C, que é pouco soluble en auga. En contacto co aire oxídase rapidamente a NO 2 , e adquire unha cor escura. Reacciona con cloro e bromo e dá haluros de nitrosilo, NOX. Emprégase no branqueo do raión. OBS: Tamén se denomina óxido de nitróxeno (II).
-
nitróxeno residual
[BIOQ]
Parte do nitróxeno non proteico, de onde se saca o nitróxeno ureico, que corresponde a compostos como o amoníaco, o ácido úrico, os aminoácidos e outros.
-
óxido de nitróxeno (I)
[QUÍM]
óxido de dinitróxeno.
-
óxido de nitróxeno (III) [N 2 O 3 ]
[QUÍM]
Gas de cor escura, que a baixa temperatura se condensa e dá un líquido azul. En estado líquido ou sólido compórtase como unha especie química definida mentres que en estado gasoso ten as características dunha mestura equimolecular de NO e NO 2 (vapores nitrosos). OBS: Tamén se denomina trióxido de dinitróxeno.
-
s
m
[QUÍM]
-
ciclo do nitróxeno
[BIOQ]
Proceso de fixación do nitróxeno do aire e a súa transformación en materia orgánica pola acción de determinados microorganismos. A conversión do nitróxeno atmosférico en amoníaco deixa este elemento dispoñible para a síntese de proteínas vexetais e animais. Outras etapas do ciclo son a nitrificación, a amonificación e a desnitrificación.
-
equilibrio de nitróxeno
[FISIOL]
Estado de equilibro, propia dos adultos, en que a inxestión de nitróxeno de orixe proteica iguala a excreción. Fálase de equilibrio de nitróxeno positivo cando a inxestión é superior á excreción e hai crecemento, e equilibrio de nitróxeno negativo no caso contrario como ocorre nalgunhas doenzas dexenerativas.