2 cal
(< lat calce)
-
[QUÍM]
-
s
m
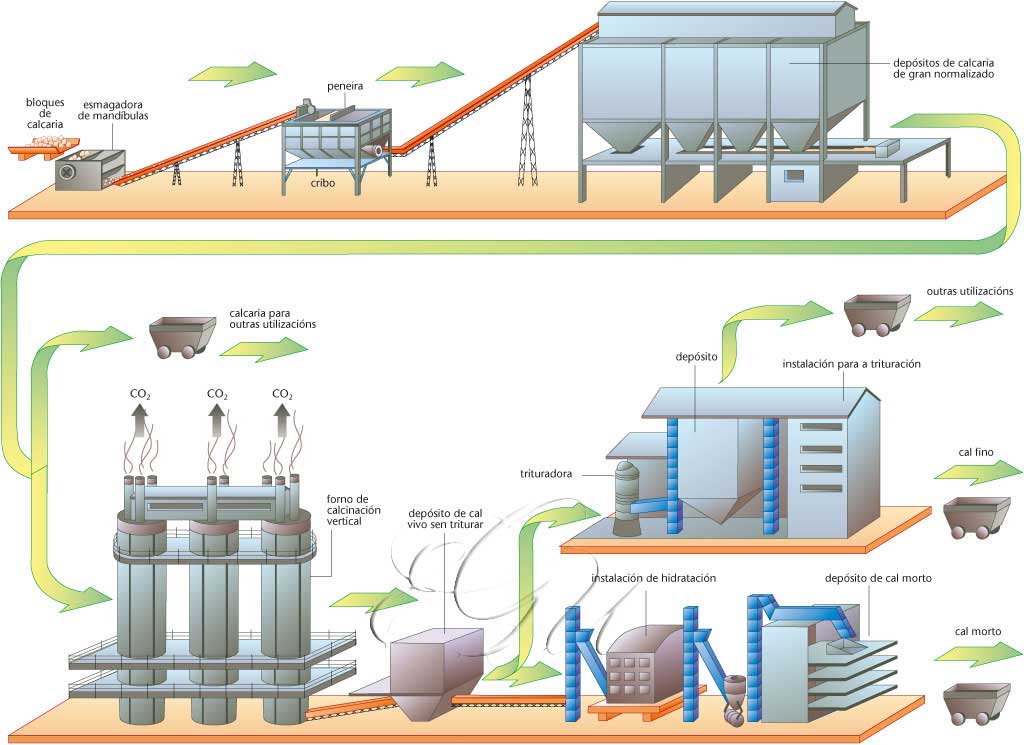
Óxido de calcio impuro, obtido por quentamento de rochas calcarias a temperaturas superiores a 1.000 ou 1.200°C nunha reacción endotérmica da forma CaCO 3 →CaO + CO 2 -42.500 cal; desta reacción deriva o concepto de calcinación. A obtención do cal efectúase en diversos tipos de fornos, con frecuencia verticais; para producións dalgúns centenares de toneladas ao día empréganse fornos rotatorios, semellantes aos da fabricación de cemento, aínda que consomen máis combustible e presentan máis limitacións no que respecta á natureza e granulometría da calcaria utilizada. O cal é un sólido branco, cun punto de fusión moi elevado (uns 2.600°C), que se volatiliza no forno eléctrico; ten unha grande afinidade pola auga, que a transforma en hidróxido con desprendemento de gran cantidade de calor. Emprégase na construción, para preparar bases alcalinas, vidro e cloruro de cal e para depurar augas duras, nas fábricas de curtidos para depilar peles, en agricultura para neutralizar os solos ácidos, e como material refractario no recubrimento de fornos de alta temperatura. Chámaselle tamén cal anhidro ou cal vivo, por oposición ao cal morto.
-
cal hidráulico
Pedra calcaria calcinada que, ademais de cal, contén ata un 17% de sílice, alumina e hidróxido férrico e que, unha vez pulverizada, non se comporta en contacto coa auga como o cal vivo, senón que solidifica e endurece dun xeito semellante ao cemento.
-
cal sodado
Mestura dos hidróxidos de calcio e de sodio que se prepara mesturando cal vivo cunha solución diluída de sosa cáustica. Emprégase na industria e nos laboratorios pola súa propiedade para absorber o dióxido de carbono.
-
cal morto
Hidróxido de calcio comercial que se obtén mesturando calcaria cocida con auga nuns dispositivos hidratadores, que poden traballar dunha maneira continua ou descontinua e que dan un produto homoxéneo e seco, que despois se pulveriza. Outras veces, na obtención de pequenas cantidades para uso inmediato ou a curto prazo, prepárase unha pasta máis ou menos espesa tratando a calcaria calcinada con auga en pequenos depósitos. Emprégase na industria química, na construción, na agricultura, como funxicida e fertilizante e na industria azucreira, entre outras. Tamén se utiliza como reactivo básico na obtención de cloruro de cal, óxido de etileno, colorantes azoicos e calcio metálico. Úsase nas perforacións petroleiras, no tratamento de augas duras e residuais e na absorción de dióxido de carbono. Mesturado con area ou pedra moída constitúe a argamasa, empregada na construción. En disolución lixeira, serve para branquear interiores e exteriores e como aglutinante de pigmentos e de colorantes. Tamén se denomina cal hidratado ou cal apagado.
-
cloruro de cal
Hidrato do sal dobre de hipoclorito e cloruro de calcio, CaCl(ClO). Chamado tamén pos de gas ou de branqueado, trátase dun material granuloso, branco agrisado, que cando está húmido cheira a cloro e que se obtén por reacción do cal morto e do cloro gasoso, a temperaturas por baixo de 40°C. A reacción é exotérmica, e procúrase disipar unha parte da calor desprendida mesturando o cloro con aire. O cloruro de cal pouco purificado emprégase como oxidante, branqueador e desinfectante. Serve tamén para preparar solucións relativamente diluídas de hipoclorito de sodio. A riqueza deste composto mídese pola cantidade de cloro que dá ao ser tratado cun ácido forte, e exprésase como contido de “cloro activo”. Este debe de ser do 35 ao 37% no produto de boa calidade. O uso do cloruro de calcio minguou moito en beneficio do hipoclorito de cal, produto máis estable e eficaz, que contén un 70% de cloro activo.
-
s
m
-
cal e pedra
[CONSTR]
Obra de cachotería constituída por cal e pedras pequenas.