ferro
(< lat fĕrru)
-
[QUÍM]
-
s
m
Elemento de transición do bloque d, situado entre os elementos dos bloques c e p na táboa periódica, de peso atómico 55,84 e número atómico 26. O elemento natural é unha mestura de catro núclidos: 54 (5,8%), 56 (91,7%), 57 (2,2%) e 58 (0,3%); coñécense cinco núclidos artificiais: 52, 53, 55, 59 e 60.
Química
A estrutura electrónica do ferro imponlle o grao de oxidación +2 (compostos ferrosos); a tensión normal que corresponde ao equilibrio FeSFe2++2e (-0,44 V a pH=0) mostra que se trata dun metal bastante electropositivo que desprazará, en particular, o cobre dos seus sales; forma tamén derivados férricos (grao de oxidación +3) e ferratos (+4 e +6). A existencia dos graos +1 e +5 é menos segura. O ferro combínase con todos os elementos non metálicos, pero non co hidróxeno. O ferro candente descompón a auga, que desprende hidróxeno, e é atacado facilmente polos ácidos diluídos; a auga pura e o aire seco non o atacan a temperatura ordinaria, pero o aire húmido e a auga aireada corróeno rapidamente, con formación de ferruxe.
Variedades e minerais de ferro
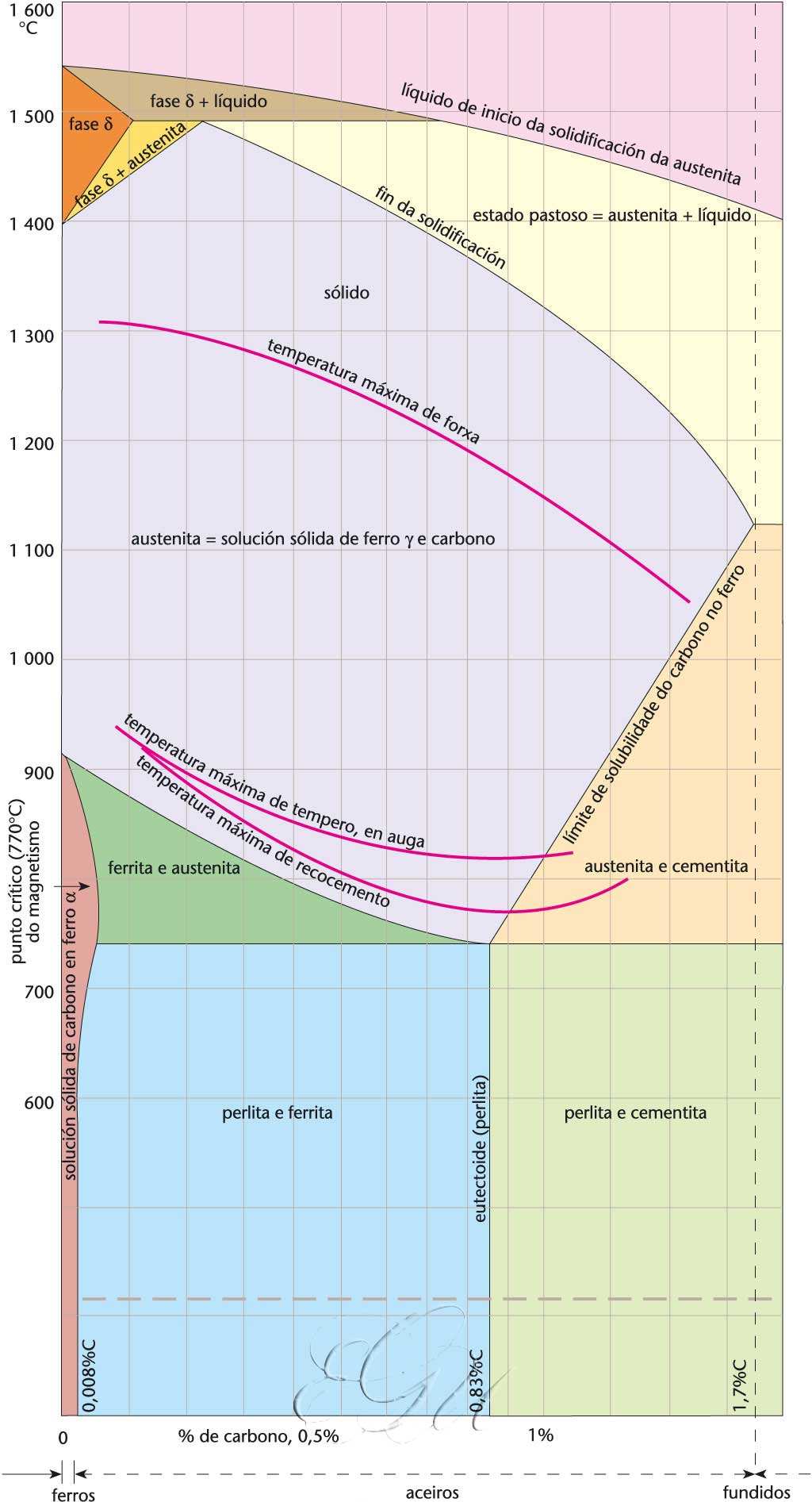
O ferro é, despois do aluminio, o metal máis abundante da natureza: constitúe o 5% da codia terrestre. Os catro chanzos da curva de arrefriamento do ferro puro parecen fixar a existencia de catro variedades alotrópicas: o ferro α ou ferrita, estable ata 768°C, fortemente magnético, o ferro β, feblemente magnético, estable entre 768°C e 900°C, o ferro γ, paramagnético, e a variedade δ, feblemente magnética, que aparece entre 1.400°C e a temperatura de fusión. O estudo das formas cristalinas e das outras propiedades físicas do ferro confirman que, de feito, soamente existen dúas variedades alotrópicas: a forma α, estable ata 900°C, e a forma γ, estable de 900°C a 1.400°C. O ferro é un metal extremadamente dúctil, tenaz e maleable a temperatura ordinaria, pero desprovisto de elasticidade. A carga de ruptura depende moito da súa orixe: varía entre 25 e 46 kg/mm2para o ferro normal do comercio, e pode acadar 143 kg/mm2para o ferro electrolítico recocido. Pódese forxar facilmente, e a 800°C o estado de abrandamento no que está permite soldalo con el mesmo. A forxa e o laminado transforman os cristais, que constitúen o ferro, fundidos nunha estrutura fibrosa que lle dá ao ferro unha gran tenacidade e un grande alongamento na ruptura (25%). Entre 800°C e 1.000°C o ferro é fráxil, pero volve ter a súa maleabilidade a unha temperatura superior a 1.000°C, e por iso os lingotes de ferro se moldean en quente (entre 1.000°C e 1.300°C). O ferro puro (ferro electrolítico ou ferro Armco) é un metal homoxéneo, bastante resistente á corrosión, dunha gran condutibilidade, que se utiliza nas industrias eléctrica e de calefacción. O ferro é un metal ferromagnético, cunha permeabilidade magnética moi elevada. Existen en estado nativo en pequenas cantidades en Groenlandia e nos meteoritos, nos que a miúdo vai aliado co níquel e aínda máis a miúdo co cobalto. Os minerais de ferro explotados son o óxido salino (Fe3O4), ou magnetita, particularmente puro, que constitúe o principal mineral de ferro sueco; o óxido férrico (Fe2O3), denominado olixisto cando cristaliza no sistema romboédrico, que ocorre a miúdo en forma de masas compactas, amorfas, que constitúen a hematites vermella ou o ocre vermello, segundo o grao de pureza do mineral; o óxido férrico hidratado (Fe2O3·nH2O), ou limonita, moi abundante en Francia, que non corresponde a un hidrato definido e é de orixe sedimentaria; o carbonato (FeCO3), ou siderita, moito menos importante, cristalizado en romboedros isomorfos da calcita, polo que se denominaba antigamente ferro espático; e a pirita de ferro e a marcasita, de fórmula idéntica (FeS2), pero de sistemas cristalinos diferentes, que se explotan sobre todo como minerais de xofre. O ferro atópase na natureza combinado con outros numerosos elementos, como o arsénico ou o antimonio, en minerais dos que non se extrae.
Obtención
O ferro é o metal que máis se utiliza; pódese obter con facilidade e pureza comercial, ten propiedades físicas e mecánicas moi variadas e pode formar aliaxes de características moi útiles. Por calcinación da siderita e redución dos óxidos de carbono (CO) no alto forno obtense o lingote de alto forno, que é unha aliaxe de ferro rica en carbono. Por descarburación é difícil obter ferro puro, sen carbono, pero existen técnicas encamiñadas a obter esponxa de ferro, como os procedementos Wiberg, Höganäs e Renn-Krupp. O primeiro destes consiste en facer caer, nun forno vertical, o mineral ferroso (rico) a contracorrente co gas redutor que se obtén por combustión incompleta dalgún hidrocarburo, co fin de conseguir unha mestura gasosa rica en óxido de carbono que, a 1.200°C, reducirá o óxido de ferro ao estado pastoso. O procedemento Höganäs utiliza magnetita concentrada e pulverizada nunhas bandexas, chamadas saggers, alternativa de capas de mineral, coque e un pouco de carbonato de calcio; as saggers colócanse nunhas vagonetas que atravesan o forno e a redución faise con gas natural, a 1.200°C. O procedemento de Renn-Krupp aproveita minerais pobres en ferro e ricos en sílice que, moídos, pasan por un forno tubular case horizontal de 100 m de longo, onde circula gas redutor a contracorrente co mineral; o produto final é unha escoura con nódulos de ferro que se poden separar por procedementos magnéticos. É posible conseguir ferro dunha gran pureza por electrólise dunha solución de sal de ferro nunha célula con ánodo de ferro ou por descomposición do ferro pentacarbonilo.
Aliaxes e clasificación
As dúas aliaxes máis importantes do ferro son o aceiro e o ferro fundido ou ferro coado. O ferro industrial pódese clasificar, segundo o método de obtención, en: ferro pudelado, obtido por oxidación do ferro fundido líquido por medio dunha escoura ferruxinosa, un procedemento xa abandonado; ferro doce, que se confunde co aceiro extra doce (menos do 0,05% de carbono) e que se obtén polos procedementos clásicos do aceiro; ferro Armco, caracterizado por unha gran pureza, propiedades magnéticas e resistencia á corrosión, que se obtén nos fornos Martin ou eléctricos; ferro electrolítico, obtido por electrólise do cloruro ferroso, que é un ferro dunha gran pureza; ferro aluminotérmico, que se produce na reacción exotérmica entre o óxido de ferro e os pos de aluminio, e que permite soldar dúas pezas de ferro; ferrocarbonilo, obtido por descomposición do pentacarbonilo de ferro (Fe(CO)5), dunha gran pureza e que se emprega para obter pezas dun alto poder magnético; e ferro reducido, obtido por redución de óxidos ou de minerais en medio gasoso redutor (H2, CO) e que ten as mesmas utilidades que o ferrocarbonilo. O procedemento de orixe estadounidense coñecido como iron process, permite a obtención directa do ferro por redución e pulverización do mineral fundido en medio redutor.
Xacementos e explotación
Os xacementos de mineral de ferro son moi abundantes, pero ás veces a explotación non rende o suficiente. O prezo do mineral depende do contido metálico, da porosidade e da composición mecánica, da porcentaxe de impurezas, das condicións de extracción, do custo do transporte, da conxunción industrial e do comercio exterior. Polo contido metálico só son economicamente explotables os minerais de lei superior ao 40%. As explotacións máis grandes do mundo son todas a ceo aberto; nos países europeos trátase unha gran parte do mineral de ferro preto da mina.
O ferro nos seres vivos
Está presente en toda a materia viva e é esencial para manter a vida; os animais superiores e os vexetais conteñen uns 5 cg por kg de peso. O organismo humano contén de 4 a 5 gramos de ferro, e manifesta unha gran tendencia a conservalo diante de calquera perda ocasional. Do 60 ao 70% deste ferro está na hemoglobina e na mioglobina. O resto almacénase no fígado en forma de ferritina e noutros tecidos, como hemosiderina. No sangue transpórtase en forma dun complexo que se denomina transferrina. Tamén forma parte da composición dalgúns sistemas enzimáticos. O contido en ferro dos alimentos é bastante variable e depende moito dos factores ambientais. Dado que o leite non contén ferro, os neonatos utilizan, ata o destete, as reservas que se acumulan nos órganos hematopoéticos durante a vida fetal. É necesario tamén para a formación da clorofila nas plantas.
A utilización do ferro na construción e as artes
A forxa do ferro, descuberta polos hititas a mediados do segundo milenio a C, propagouse por toda Europa un milenio máis tarde, a causa da influencia de diversos pobos (fenicios, gregos, escitas e cimerios), e tivo un incremento extraordinario na cultura de La Tène, onde se elaboraron con ferro armas e todo tipo de utensilios para a agricultura e a decoración. Tamén foi bastante abundante nas civilizacións etrusca e ibera. Na Idade Media, utilizouse como elemento de protección das portas e despois evolucionou cara á constitución de elementos decorativos. O desenvolvemento destas aplicacións de ferro forxado debeuse á invención do martelo hidráulico e das técnicas da estampación. A forxa foi idónea para facer as reixas traballadas e esveltas, propias do gótico florido, ou os preciosismos do Renacemento. No s XVII apareceron os primeiros balcóns. As formas de orixe medieval perduraron na arte popular e en todo tipo de utensilios. No s XIX chegou a ser progresivamente un elemento importante, xa non soamente decorativo, senón construtivo, na arquitectura. -
cloruro de ferro(II) [FeCl 2 ]
Substancia de cor verde que se obtén pola acción do ácido clorhídrico sobre o ferro. Tamén se coñece como cloruro ferroso.
-
cloruro de ferro(III) [FeCl 3 ]
Sólido vermello que se obtén pola acción do cloro enriba do ferro e que se emprega para coagular o sangue. Tamén se coñece como cloruro férrico.
-
óxido de ferro(II) [FeO]
Protóxido de cor negra, que se obtén a alta temperatura por redución do óxido férrico; o hidróxido correspondente é un precipitado verde. Tamén se coñece como óxido ferroso.
-
óxido de ferro(III) [Fe 2 O 3 ]
Sesquióxido moi abundante na natureza, do que a ferruxe é un hidrato. Obtense por calcinación do sulfato ferroso, e neste caso utilízase, con diferentes nomes (colcótar, vermello de Inglaterra ou vermello de Venecia), para puír o vidro ou as armas; o hidróxido correspondente é un precipitado avermellado. Tamén se coñece como óxido férrico.
-
óxido salino de ferro [Fe 3 O 4 ]
Óxido que constitúe a pedra de imán natural; obtense artificialmente por combustión do ferro ou por acción do vapor de auga, baixo a forma dun po negro. Considérase como unha combinación dos outros dous óxidos. O óxido férrico tamén se pode combinar con outros óxidos, ademais do óxido ferroso, e pode dar ferritas, pertencentes ao grupo das espinelas, que permiten obter os ferratos por oxidación. Tamén se coñece como óxido magnético ou magnetita.
-
sulfato de ferro(II) hidratado [Fe(SO 4 )·7H 2 O]
Sal que se presenta en forma de cristais verdes e que se obtén por acción do ácido sulfúrico sobre o ferro. Emprégase como redutor. Tamén se denomina sulfato ferroso hidratado ou vitriolo verde.
-
sulfato de ferro(III) [Fe 2 (SO 4 ) 3 ]
Sal que se obtén por acción do ácido sulfúrico sobre o óxido férrico; as súas solucións son de cor laranxa. Combínase coas materias orgánicas e dá compostos imputrescibles, razón pola que se emprega para depurar as augas industriais e as redes de sumidoiros.Tamén se denomina sulfato férrico.
-
sulfuro de ferro(III) [FeS]
Composto que se obtén sinteticamente e que serve para preparar o ácido sulfhídrico. O bisulfuro (FeS2) é a pirita natural que se emprega para a fabricación do ácido sulfúrico.
-
s
m
- s m
-
s
m
Márca que se lle pon ao gando cun ferro candente.
Ex: Baixaron os cabalos do monte para poñerlles o ferro.
-
s
m
[BÉL]
-
Arma de fío.
-
Punta metálica de certas armas.
-
Folla dunha espada, dunha daga ou dalgunha outra arma de fío. Na tradición oral recóllense ditos como: “Cargado de ferro, cargado de medo. Quen xoga co ferro, xoga co demo.”
-
-
s
m
[DEP]
Pao de golf que ten a cabeza de metal.
-
s
m
[MAR]
áncora.
-
s
m
Termo do verbo dos daordes, ou xerga dos telleiros, que designa a ferramenta para amasar o barro.
-
ferro de pasar
[TECNOL]
Instrumento que consiste nunha prancha metálica, normalmente de forma triangular, e unha asa pola que se agarra, que, convenientemente quentada, serve quera quitarlle as engurras á roupa. O seu quentamento facíase mediante o contacto cunha fonte de calor ou queimando carbón no seu interior, que se substituíu por unha resistencia eléctrica. O ferro de pasar eléctrico ten normalmente un termostato e un selector de temperatura manual para regular a temperatura adecuándoa ao tipo de tecido que se quere alisar; o de vapor leva, ademais, un depósito de auga que, vaporizada, humedece a roupa no momento de pasalo sobre ela.
Frases feitas
-
De ferro. Que é moi resistente.