orbital
(<órbita)
-
adx
Relativo ou pertencente á órbita.
-
[QUÍM/FÍS]
-
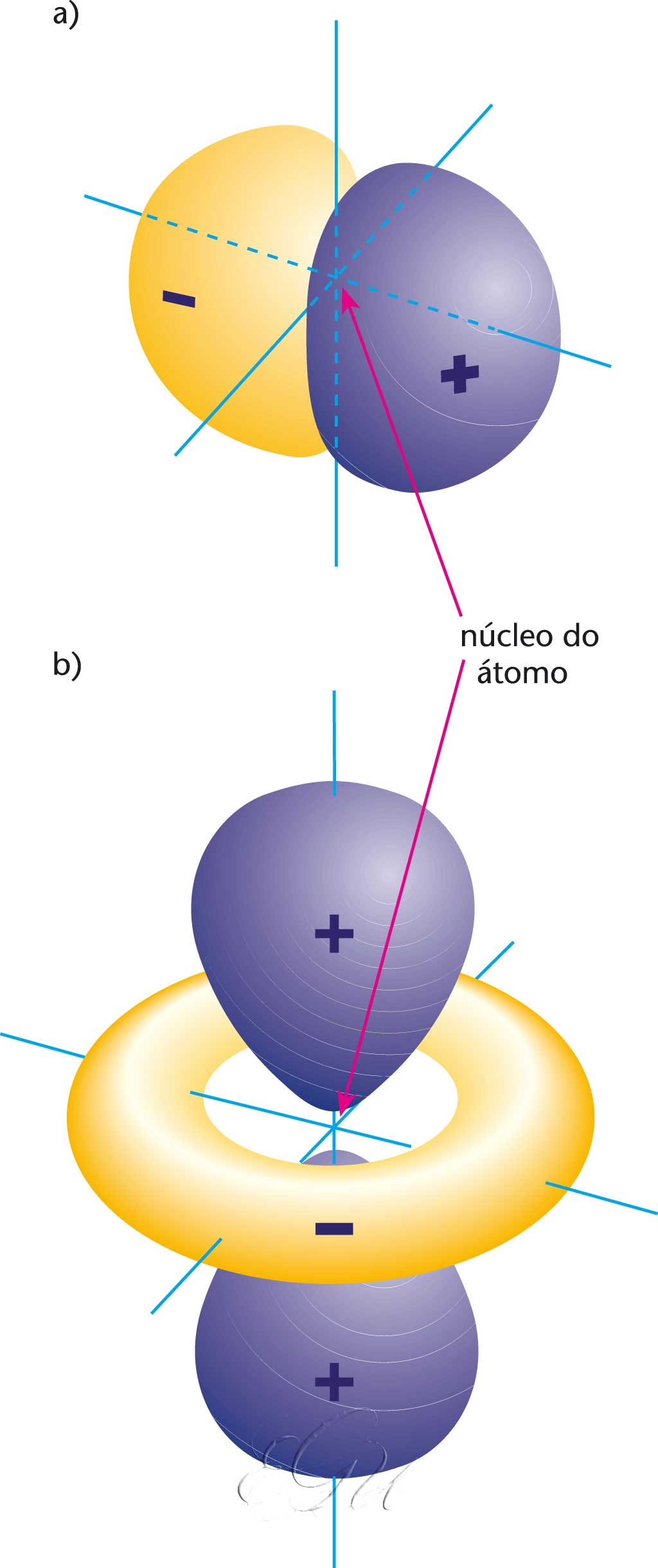
orbital atómico
Cada unha das funcións, solución de ecuación de Schrödiger, que describen o estado estacionario dun electrón que forma parte dun átomo. O concepto de orbital foi introducido a finais da década de 1920, coincidindo co desenvolvemento da mecánica cuántica, que permitiu superar todas as dificultades que o modelo do átomo de Bohr presentaba. O produto da función de onda pola súa conxugada representa a probabilidade de atopar o electrón en cada punto do espazo. Os orbitais defínense mediante tres números cuánticos: n, número cuántico principal, que determina a enerxía do orbital e pode ter valores 1, 2, 3...; l, número cuántico angular, que representa o momento angular do electrón debido ao seu movemento e toma os valores 0, 1, 2...(n-1), que orixinan, respectivamente os orbitais denominados s, p, d, f,..., e m, número cuántico magnético, que toma os valores 0, ±1, ±2, ±3,..., ±l. Así, para un número cuántico principal n poden existir n 2 orbitais. En ausencia de campo externo, todos os orbitais que teñen os números cuánticos n e l iguais son da mesma forma e enerxía, e dise que son dexenerados. Ademais dos orbitais mencionados, existen os denominados híbridos, que están formados por combinacións lineais de orbitais con valores de l diferentes, e son de grande importancia para a formación do enlace químico. Cada orbital pode representar dous electróns, sempre que estes difiran entre eles no valor dun cuarto número cuántico m s , denominado de spin. Este feito é de grande importancia para o establecemento da configuración electrónica dos átomos polielectrónicos.
-
orbital molecular
Cada unha das funcións de onda, solución da ecuación de Schrödinger, asociadas a un electrón que forma parte dunha molécula. Presentan as mesmas características matemáticas que os orbitais atómicos. Son de natureza policéntrica e constitúen neles mesmos unha interpretación do enlace químico. A descrición da estrutura molecular mediante o uso de orbitais moleculares é coñecida como teoría do enlace dos orbitais moleculares. Dada a imposibilidade de resolución analítica da ecuación de Schrödinger para sistemas con máis dun electrón, é necesario o uso de métodos aproximados para a obtención de orbitais moleculares. O máis empregado destes métodos é o CLOA (Combinación Lineal de Orbitais Atómicos), que considera o orbital molecular como a combinación lineal de orbitais atómicos dos átomos constituíntes. De acordo co seu sistema de simetría respecto ao eixe de enlace, clasifícanse os orbitais moleculares en σ (de simetría cilíndrica), π (de simetría binaria) e δ (de simetría cuaternaria). Doutra banda, a combinación lineal de dous orbitais atómicos orixina sempre dous orbitais moleculares, denominados enlazante e antienlazante. O orbital enlazante é de enerxía máis baixa que os orbitais atómicos que o orixinan, mentres que o antienlazante é de enerxía máis alta.
-
orbital atómico